阅读:0
听报道
色
中文一个“色”字,有多种意思。英文的“color”,有多学科的解读。
从物理学角度,大家熟知牛顿(1642-1727)于1672年用三棱镜实验研究颜色的光学特征。从生物学角度,色觉是神经系统对外界的反应,牛顿曾于1704年提出人如何感知颜色的想法:光振荡以不同比例作用于视神经,传入大脑而导致人对色的感觉不同。可以说,牛顿在感觉神经生物学方面有先驱的想法。
眼睛是人类观察世界的重要器官,而科学家对眼睛的研究也是人类理解自身的渠道之一。科学家们研究眼睛,以期理解视觉、感觉,甚至人类的大脑。
因为对颜色的感知始于眼睛、最终成于大脑皮层,所以需要在多个层面研究色觉,本文限于眼睛中第一级感光细胞对色觉分辨的分子基础,仅这一个层面就有很多科学家前赴后继的工作。
眼见不为实
不同方法和设备只能检测物质世界的部分特性。视觉系统并非照相机,而是对外界信号加工后获得对特定种属动物有意义的信息。现存感觉系统也是演化过程中选择的结果,较为实用地获得物种常遇见的外界信息。眼和脑的局限导致我们的视觉系统不能完整和准确地反映外界的物理实际。
因此,眼见并不一定为实。
视错觉(visual illusion)可以显示视觉系统不是客观的简单影射。绝大多数人都有视错觉,如果少数人没有这种视错觉,其中有些人可能是因为基因的变化,研究人员会感兴趣收集其血样,通过检测DNA的变化,研究是否有基因变化。
第一个图中可以显示佛家所谓外界没动、观察者的心在动。中两个圆圈物理上没动,而多数人觉得它们在相对运动(一个顺时针、一个反时针)。

第二个视错觉的图,在一般人看来,立方体上面正中小方块呈“褐色”,而在立方体左侧面正中的小方块呈“黄色”,认为这两块的颜色差别很大。而实际上,读者不妨做个简单的实验,将图像拷贝下来后把这两小方块分别分离出来,可以发现它们的颜色完全一样:褐色。

第三个错觉,一般人看到蓝色和绿色两个颜色的螺旋,其实这“两个”颜色在物理上是完全一样的颜色。

第四个视错觉,需要动画才能看到,读者到。
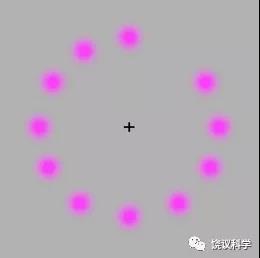
物理现实是:环绕加号的紫色原点在顺时针方向逐个消失再出现。但是,当人盯着中间的加号一段时间后,可以看到一个浅绿色圆点顺时针方向运动(不是消失和再现,而是圆点绕圈运动)。如果你不相信这是你的错觉,可以在出现绿色圆点后移动你的头,绿色圆点会消失,等你再盯着加号后会再现,似乎由你可以不动手而靠遥控掌握外界。当然这是你的感觉,非外界现实;如果不能区分自己的感觉和外界的现实,那是精神病。
这些视错觉都是我们视觉系统处理信号的机制所造成,其中有些机理不明。
视觉与光感
视觉与光感不同。植物有光感、有些细菌也有光感,但它们不能形成动物一般的视觉。
植物感光能力有时很奇妙。植物可以通过检测日光中不同波长的光、每日不同波长光照的时间,知道冬天变成春天、秋天变成冬天,从而做出相应的季节性变化。植物感光的分子已经发现多种,一般是蛋白质和小分子参与植物光反应。植物的感光蛋白只有一种和动物相似,即cryptochromes,是近二十年的一个有趣发现。
动物界有多种不同眼睛和视觉系统,在进化中视觉系统独立地发生过四十次以上。不同动物视觉特性不一样,蜜蜂能感知偏振光。
人的视觉系统从位于外周的眼睛开始,眼睛的视网膜(retina)从外界获得信号后稍作加工、传递到丘脑的外侧膝状体(lateral geniculate nucleus,LGN)、再到大脑的视皮层(visual cortex),成为视觉通路。
人也有不形成视觉的感光系统。瞳孔对光反射指光强度增加时,我们的瞳孔缩小。这一反应即使用了我们的视觉系统,也可能用了不能形成视觉的感光系统,如存在于视神经节细胞的cryptochromes和melanopsin。
眼内的神经细胞
达芬奇曾对眼睛和视觉系统感兴趣。
笛卡尔(1596-1650)不仅是哲学家、数学家,现在也可以说是神经生物学家。他将神奇的大脑回归为物理基础,提出神经纤维是通过水力传输信息。神经生物学学者可以开玩笑说,笛卡尔所谓“我思故我在”的意思是强调神经系统的重要性。

笛卡尔在1637年的《方法论》一书中曾显示眼睛的解剖、去世12年后出版的《论人》一书中绘制了视网膜上的神经细胞(后来称为视杆细胞)。
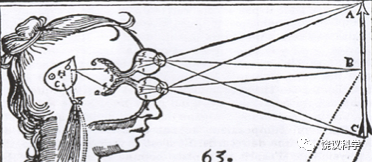
笛卡尔也曾描绘光通过眼睛晶状体投射到视网膜、视网膜收集的信息通过视神经从眼睛投射到大脑的步骤。
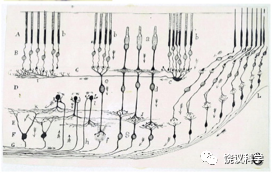
眼睛由多种细胞组成。人的眼球从前到后有角膜、晶状体(英文更为反映其作用称其为透镜lens)、水晶体(vitreous body)、视网膜。视网膜神经细胞通过视神经(optic nerve)向脑投射。视网膜内有三级神经细胞传递光信号,第一级为感光细胞(photoreceptors),第二级为双极细胞(bipolar cells),第三级为视神经节细胞(retina ganglion cells,RGC)。视网膜还有不直接传递信息、而参与修饰加工的水平细胞(horizontal cells)和无突起细胞(amacrine cells)。这里显示一副西班牙解剖学家Santiago Ramón y Cajal (1852 –1934)画的图。
传统认为,人类的第一级感光细胞有两种:视杆细胞(rods)和视锥细胞(cones)。1675年Anton van Leeuwenhoek (1632-1723)可能观察到了感光细胞,而其一百多年后的Gottfried Reinhold Treviranus (1776–1837)描述了感光细胞。十九世纪,德国的Rudolph Albert von Kolliker (1817 -1905)与Max Schultze(1825-1874)清楚地知道视网膜细胞的分层和感光细胞。Schultze画的视杆和视

锥细胞如图。
现代的电子显微镜拍摄了漂亮的视杆细胞和视锥细胞照片:
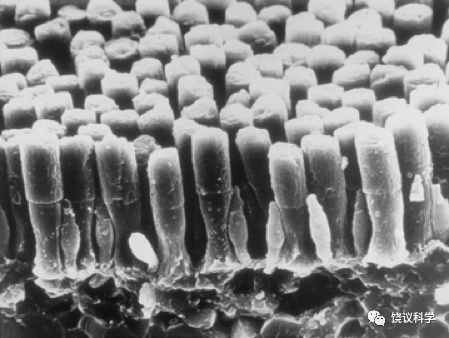
视杆细胞有一段长长的杆状部分,这是视杆细胞的“外段”(outer segment),起感光作用。视杆细胞的数量远多于视锥细胞:人有1.2亿视杆细胞,而仅6百万视锥细胞。两种细胞在视网膜的分布不同,功能不同。视杆细胞主要是感知明暗,视锥细胞感受不同的颜色,是辨别色觉的第一级细胞。
Hecht等(1942)和van der Velden (1946)发现感光细胞对光的敏感性非常高,单个细胞可以对单个光子有反应。他们的工作在1979年为Stanford大学的Baylor、Lamb、和Yau(游景威)用更精确的技术所验证。在认知上,人可感知5到8个光子。
有个夸张的小故事。德国海德堡大学生理学教授Willy Kühne(1837-1900)在1878年发现:让一只兔子在暗室内注视阳光射入的窗口,一段时间后处死兔子,固定其视网膜,可以看到窗子的印记。当时很轰动,以为这可以用来破案。如果被谋杀的人的视网膜都留下如此强烈的印记,找到凶手,就不怕凶杀现场没有证人,只要被谋杀的人最后一眼看到了凶手就可以。当然一般信号没这么强,这一发现并无实际应用价值。

视网膜的感光蛋白
1851年,德国的Heinrich Müller发现视网膜中视杆细胞呈红色,认为是血液中红细胞的血红蛋白所造成(Müller,1851;Ripps,2008)。
1877年,德国生理学家Franz Böll (1849–1879)发现,在暗中视杆细胞为红色,见光20秒后经过黄色、60秒后成为无色,他的解释是视杆细胞中存在色素,他称为“红色物质”,见光后起反应而漂白,在暗处2小时后复原为红色。他排除了死亡与漂白的关系、也排除了血液与漂白的关系。Böll提出视杆细胞外段含特殊的物质,通过光化学过程,将信号传到大脑(Böll,1871;Wolf,2001;Ripps,2008)。可惜,Böll发表论文后因肺结核而不能继续工作,于30岁英年早逝。
Böll的论文发表后不久,德国海德堡的Kühne开始继续其研究。Kühne以前曾发现胰蛋白酶,而1877至1882年间集中时间和精力研究视网膜,发表22篇相关的论文(Wolf,2001)。Kühne将Böll的视杆色素称为“视紫”(visual purple),Kühne发现光漂白后视杆细胞的在黑暗中还原为紫色还需要另外一种细胞:视网膜色素上皮细胞(retinal pigment epithelium,RPE)。只有在RPE存在的情况下,被光漂白的视杆细胞才能在暗中重新成为紫色;漂白和复原都无需血液循环,从死的动物取出的视网膜就能够进行,肯定与血红蛋白无关(Wolf,2001)。
Kühne发明了提取视紫的方法:在明矾溶液中,视网膜和RPE分开,视网膜硬化,方便分离视网膜,然后加入胆盐溶液,视杆细胞溶解,将视紫释放到溶液中。因视紫对热的敏感、不能过透过半透膜、可溶于硫酸铵,Kühne推测它是蛋白质。Kühne发现视紫分子本身就对光有反应,能被光漂白。他明确提出:光能解构视紫,光化学反应产物刺激视神经(Wolf,2001)。Kühne的工作将人类对视觉的理解推进到分子水平,落实到特定分子。
Kühne发现的视紫,是世界上第一次发现细胞膜上的蛋白,后称为“视紫蛋白”(rhodopsin),中文教科书仍译为“视紫红质”。
既然视紫蛋白是蛋白质,那么就是多个氨基酸按特定顺序连接而成。二十世纪,经过多个实验室的研究,逐步获得视紫光蛋白的氨基酸部分序列。1983年,美国南伊利诺大学的Hargrave等和苏联的Ovchinnikov等分别通过分离肽段,经过分析获得视紫蛋白的全长序列。
当时已知如果连续出现19到21个左右的疏水氨基酸可以组成跨细胞膜的a螺旋,从视紫蛋白的氨基酸序列可以预计七个跨膜区域,即所谓“七重跨膜蛋白”。在生物化学上,先发现一些受体(如肾上腺素能受体)与G蛋白偶联,所谓“GPCR”(G蛋白偶联受体),对感光细胞的研究也发现视紫光蛋白是GPCR。视紫蛋白是被光子激活的GPCR,而肾上腺素能受体等是被化学分子激活的GPCR,这些七重跨膜的GPCR在本质上相似。
了解视紫蛋白一级结构(氨基酸序列)后,进一步需要知道其三维的空间结构。视紫蛋白与其他跨细胞膜的蛋白质一样,以前很难通过X线衍射分析其晶体结构。1997年,日本的Kimura等在《自然》发表论文,用冷冻电镜在3埃的分辨率解析了细菌视紫蛋白的结构。1999年,法国的Belrhali等在1.9埃分辨率解析了细菌视紫蛋白的三维结构。这些结果都清晰地显示了七重跨膜区域。2000年,美国的Palczewski、Stenkamp与日本的Miyano等在《科学》合作发表论文,他们解析了眼中视紫蛋白的三维结构,并显示视黄醛结合位点。
维生素A与光化学
动物感光细胞的光化学反应不仅需要蛋白质,还需要其他分子。
十九世纪Kühne在研究视网膜漂白过程发现,从紫色、橘黄色、黄色到无色,但黄色不可能是视紫物质造成的,应该有另外一个分子,其吸收波长短于视紫物质(Wolf,2001)。后来的研究揭示黄色是视紫蛋白结合了全反型视黄醛所致。
视黄醛的发现与夜盲症以及维生素A有关。几千年前人们就注意到有些人在暗光下视力不如一般的人,而且发现有些夜盲与营养相关(Wolf,2001)。希波克拉底(公元前460-325)建议夜盲症患者吃肝。1913年,威斯康辛大学的Elmer McGollum与Marguerite Davis、耶鲁大学的Thomas Osborne与Lafayette Mendel在研究老鼠生长需要的营养因素过程中发现维生素A。1925年,丹麦哥本哈根大学卫生研究所的Fridericia与Holm证明维生素A参与视光漂白后在暗中的复原,并提出这可能解释维生素A与人的夜盲症关系。Yudkin于1931年证明视网膜含维生素A。
犹太裔美国科学家George Wald(1906-1997)于1927年在纽约大学毕业后进入哥伦比亚大学,研究生第一年听过摩尔根和Selig Hecht(1892-1947)的课,后选Hecht为导师。犹太裔的Hecht当时是世界主要视觉生理学家,1919年曾提出光感受的基本过程:光敏感物质S,经光解后为P和A,在暗中复原为S。Wald研究生课题是果蝇视觉,发现果蝇与人的视觉有相似的方面,1932年获博士学位(Dowling,2002)。
Wald毕业后到德国做博士后,分别师从Otto Warburg(1883-1970,因研究细胞氧化还原过程的分子而获1931年诺贝尔生理奖)、Paul Karrer(1889-1971,因研究胡萝卜素及其与维生素A的关系获1937年诺贝尔化学奖)、和Otto Meyerhof(1884-1951,因研究糖酵解而获1922年诺贝尔生理奖)。Wald在三个实验室学习了不同的思想和分析方法(Dowling,2002)。
Wald研究生期间学习的是他以后要研究的问题:视觉,而博士后期间学习的是他进行研究所需要的方法:生物化学。他的研究是视觉的生物化学,分析参与视觉的分子、以及分子在视觉过程中的变化。
Wald在Warburg实验室学会用光谱分析,发现视紫蛋白相连的分子可能是维生素A。Warburg建议Wald师从做胡萝卜素的Karrer,Wald在Karrer实验室检测牛羊猪的视网膜,确认都含维生素A(Wald,1933)。他再到德国犹太科学家Meyerhof实验室,发现在暗中和光照后,维生素A相关的分子有所不同,并能双向改变,从而提出视循环(visual cycle)。
1934年Wald回到美国,从此在哈佛大学继续研究维生素A与视觉的关系(Wald,1935,1968),他和其他科学家(包括他的第二任妻子Ruth Hubbard、合作者Paul Brown)几十年的工作推进了对视网膜光化学的理解,他们发现的视循环,用现在的语言表述为:视黄醛在视网膜有两种光学异构体,全反型(all-trans retinal)与11顺型(11-cis retinal)。11顺视黄醛与视紫蛋白形成共价键结合,结合位点是视杆光蛋白的一个赖氨酸。在黑暗时这一构型稳定,而光照时,11顺视黄醛变构为全反型视黄醛,脱离视紫蛋白。Wald获1967年的诺贝尔生理或医学奖。
视循环也称视紫蛋白循环、或视黄醛循环,目前仍然研究未完(Smith,2010),视黄醛顺反光学异构的速度很快,在10-13秒内发生。光化学变化也不仅一步,而有多步。
脱离了视黄醛的视紫蛋白本身构型改变,触发其下游的 G蛋白复合体,复合体有三个亚基(a,b,g),解离后Ga亚基结合并激活磷酸二酯酶,后者降解cGMP(Arshavsky等,2002)。在脊椎动物视网膜,感光细胞的关键第二信使分子是cGMP。1985年苏联科学院生物物理研究所的Fensenko等在《自然》发表的论文,用膜片钳技术证明蛙的感光细胞及其外段能被cGMP开放阳离子通道,使钠离子和钙离子流入细胞内,兴奋感光细胞。
感光细胞在电生理上几点特别:一般神经细胞被刺激时多半被激活,产生动作电位。而脊椎类的感光细胞,首先不能产生动作电位;其次,在被光刺激的时候,不是被激活,而是被抑制。在黑暗中,感光细胞释放神经递质谷氨酸(glutamate)。在大脑中谷氨酸一般只兴奋下级神经细胞,而视网膜感光细胞释放的谷氨酸对下级的双极细胞有两种不同的作用:或兴奋、或抑制,取决于双极细胞表面的谷氨酸受体的不同。所以,被谷氨酸兴奋的双极细胞,在光照后因为感光细胞释放谷氨酸减少而相对被抑制;被谷氨酸抑制的双极细胞,在光照后因为谷氨酸减少而相对被兴奋。
色觉的三原色理论
英国科学家胡克(Robert Hooke,1635-1703,弹性定律的提出者)于1665年提出:光照到视网膜的角度不同导致不同的颜色。胡克对色觉的推想是错的,而其长期竞争对手牛顿有关色觉的想法在原则上是对的。
牛顿与胡克因为万有引力和光学有过多个发明权的争论。牛顿可能因此才等到胡克去世以后的1704年发表《光学》一书。牛顿对人脑感受色觉的理解是“May not the harmony and discord of colours arise from the proportions of the vibrations propagated through the fibres of the optick nerves into the brain”,提出光振荡的比例通过视神经传到大脑。在生物学上,有很多简单的想法,大家都想的到、但不容易证明;有些想法,如牛顿对于色觉的想法并不容易,需要过几百年才得以证实和发展。而孟德尔在有实验证据的情况下推出的理论,因为思想超前所以需要几十年才被人们广泛接受:生物学也有时有很难、很超前的想法。
三原色最初是George Palmer于1777年提出:“每束光由三种、也仅有三种组成,黄、红、蓝……视网膜表面有三种不同的颗粒,类似于三种光;每种颗粒为相应的光束所动”。其中,有关光只有三种成分的物理学理解是错误的,而对视网膜的假设与现在的理解有想通性。
Palmer的文章常被忽略,Young-Helmholtz理论为三原色的主线。
英国科学家Thomas Young于1801年宣读,1802年发表的“光和色的理论”。在引用牛顿在《光学》中对颜色和色觉的讨论后,Young提出,不可能在视网膜的光敏感点含有无穷的颗粒,每一颗粒与对应的光同步振荡,所以需要提出有限的颗粒数,比如三原色(three principal colours),红黄蓝。每一种的振荡或多或少偏离完全同步。视神经的每根纤维可能有三部分,分别对一种原色敏感。至于为什么是这三种颜色,他当时只是猜测性地将三种原色分布在可见光较广的范围内。Young被很多人认为是第一位提出色觉三原色。如果认为Palmer对光的物理理解错误,所以影响其三原色理论的准确性,也可以认为Young在对光的连续性正确理解的基础上,提出视网膜为基础的三原色是第一次正确地理解三原色。
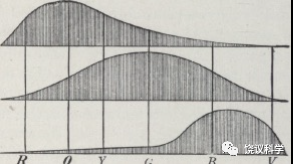
英国物理学家麦克斯韦(James Clerk Maxwell,1831-1879)和德国生理学家赫姆霍兹(Hermann von Helmholtz,1821-1894)发展了Young的色觉理论。麦克斯韦还在1861年显示了彩色照相的可能。赫姆霍兹对光的生理学有深入和细致的讨论,知道视神经的电生理。对于色觉,他发展了Young的理论,提出有三种视神经,分别对红、绿、紫最敏感,各种颜色的光对这三种视神经有不同程度的激活,导致不同的色觉。他指出理论上无法确定哪三个颜色是三原色,只能从色盲来确定。
人的视锥细胞到底有几种、分别对什么波长的光最敏感,到1964年才由美国霍普金斯大学的Marks、Dobelle和MacNichol所确定(Marks et al.,1964)。实际上,人类三种视锥细胞最为敏感的波长分别为:564 nm、533 nm和437 nm。它们分别接近黄、绿和紫,根本没有对红色最为敏感的细胞,所以现在也称为长(L)、中(M)、短(S)波长的视锥细胞。用红黄紫或红黄蓝是习惯用法,科学上不准确。不同的动物,不仅色觉细胞种类不同,所含光蛋白(opsins)敏感的波长也不同。果蝇有对紫外线敏感的感光细胞。
互补原则和核酸杂交
在讨论如何找到色觉的分子基础以前,我们需要理解分子生物学一个基本概念、以及由此衍生的核酸杂交技术。
1953年,美国遗传学家James Watson与英国物理学家Francis Crick合作,提出DNA的双螺旋模型。这一模型最重要的特点是:两条相互环绕的核酸链所含核苷酸(A、C、G、T)通过氢键与相对链上的核苷酸形成特异性的配对:A对应T,G对应C,也称碱基配对。如一条链是AAGTCTGGA,其对应的链就是TTCAGACCT。这一互补原则(complementarity),有重要生物学意义,遗传信息通过模板拷贝而传递下去。
科学家们利用互补原则的碱基配对特异性,发明了新的技术:分子杂交(molecular hybridization)。用同位素标记一条链的DNA,作为探针,通过探针与互补链的结合而找到另外一条链。如果用双链DNA做的文库,在一定条件下两条链松开,那么,一条短片段做的单链探针可以找到文库中相应的DNA。
要求两条链100%碱基对配对的互补可以用高保真的条件达到。而有些基因在不同种类进化后,不会百分之百一样。比如人与牛的同一基因有一些差别。低于百分之百互补的两条DNA链,在一定条件下,也能杂交。需要降低杂交时对互补的要求,所谓低保真度杂交(low stringency hybridization)。降低杂交的保真度可以通过降低杂交进行时的温度、或增加溶液中的盐来达到。也就是用牛的基因得到的DNA探针,通过低保真杂交可以在人基因文库找到人的基因。
色觉的分子基础
Wald研究过不同色觉的细胞,发现它们都用视黄醛,但所用的光蛋白不同。那么,如何找到人类对不同颜色反应的光蛋白?这是1980年代初期美国Stanford大学研究生Jeremy Nathans(1958-)的工作。
在自己父亲参与开拓的分子生物学黄金时代,Jeremy Nathans加入生物医学研究。1980年代,他在Stanford大学念研究生的导师为David Hogness。Hogness从1960年代末起不断推进果蝇的分子生物学技术,同时研究了果蝇发育的基因。但Jeremy Nathans加入Hogness实验室不是做果蝇,而是分析人的色觉蛋白的基因。
1982年已有牛视紫蛋白的部分氨基酸序列发表了。1983年美国的Hargrave和苏联的Ovchinnikov分析获得了牛视紫蛋白的全长氨基酸序列。已知主管明暗的视紫蛋白后,怎么样拿到色觉的光蛋白?
1983年,Nathan与Hogness在《细胞》的论文清晰地介绍了他们的策略。他们推测感色觉的光蛋白(我们这里姑且称为视锥光蛋白,因为应该是存在于视锥细胞中)与视紫蛋白有部分序列相似性,所以可以通过视紫蛋白找到视锥光蛋白。Nathans的研究用了四步。第一步,通过他们研究开始前得知的部分牛视紫蛋白序列,找到其编码的cDNA而预测其全长蛋白质的氨基酸序列;第二步,用牛的视紫蛋白基因寻找人的视紫蛋白基因;第三步,用视紫蛋白基因寻找视锥光蛋白的基因;第四步,确定每个视锥光蛋白对应什么颜色。
Nathans的第一步是用分子生物学方法做的,而Hargrave和Ovchinnikov是用生物化学。生物化学方法比较经典,而且到今天都很有用,有时还起不可替代的作用。但掌握好生物化学方法比较难,有了分子生物学以后,在有些方面可以替代一些(但非全部)生物化学的方法。比如,在得知部分氨基酸序列的情况下,制造DNA探针筛选含全长基因的DNA文库而找到相应的全长基因。这是80年代很热门的方法,当时一般实验室专注一个或少数几个蛋白质及其基因,而日本的Shosaku Numa用此方法研究了很多重要蛋白质的基因。Nathans和Hogness依据Hargrave等(1982)报道的牛视紫蛋白部分序列,制造DNA探针,通过筛选获得编码视紫蛋白的cDNA,得以预计视紫蛋白全长氨基酸序列,Nathan和Hogness的这篇文章于1983年发表在《细胞》。
第二步,Nathans用牛视紫蛋白基因的序列设计探针,在人的cDNA文库中寻找人的视紫蛋白。假设牛视紫蛋白的一段序列是TAGTACTACTTGT,那么人的视紫蛋白相应这一段可能有些差别,不是百分之百相同。通过降低杂交要求,可以用牛的视紫蛋白基因做探针来找人的视紫蛋白基因。Nathans称他用了自己的“种系发生细胞”制造人基因文库的DNA。Nathan和Hogness于1984年的论文报道他们找到人的视紫蛋白基因,其氨基酸序列与牛的视紫蛋白相似性为93.4%。
第三步,用人的视紫蛋白基因DNA做探针,寻找视锥光蛋白的基因。这是基于推测视锥光蛋白也应该与视紫蛋白有一部分序列相似性。这样也是用人的视紫蛋白基因做探针,通过低保真度杂交,找到其他三个基因。Nathans等(1986)发现它们编码的基因相互有高度的相似性,而与视紫蛋白的相似性仅41%。
如何确定这三个基因相应什么颜色?Nathan等在1986年的第二篇《科学》论文报道,他们通过分析色盲患者的DNA,看患者哪段DNA出现问题,相应于Nathans获得的哪个基因,从而确定基因与色觉的对应关系。这是人类遗传学与分子生物学的交集。
这一系列漂亮的实验,有一些合作,几年之内主要工作以一个研究生Nathans为主。他的工作成为色觉分子研究的里程碑。
结语
色觉的第一级在视网膜的三种视锥细胞,它们分别对不同的颜色有最大的反应,相应三个最佳波长,它们并非一般所谓红绿蓝的三原色,而是黄绿紫,这是真正的三原色。
视锥细胞中参与感光反应的是视锥光蛋白与视黄醛,其中吸收光的是视黄醛、但视锥光蛋白影响其对不同颜色的反应。人的视网膜有三种视锥光蛋白,其基因于1986年用分子生物学方法获得,基础是首先通过生物化学获得了视紫蛋白的部分序列。一般各种颜色的光不同比例地刺激三种视锥细胞,信号在视网膜有一些加工后,传入大脑,经过更复杂的加工,而获得高级的认知。
对于色觉的第一级分子理解是否完结,也不一定。以前认为感光细胞只有第一级的视杆细胞和视锥细胞,1998年Provencio等发现视网膜第三级的视神经节细胞有少数细胞含另一种光蛋白:melanopsin(黑光蛋白)(Provencio等,1998,2000)。这些细胞可能参加光感(Hattar等,2002;Berson等,2002)。而2012年底Stanford大学心理系的Horiguchi等(2012)提出人视网膜在边缘区域可能有对三色以外第四色敏感的细胞,也许是含melanopsin的细胞。
而更近的研究发现,光蛋白可能在一些细胞和系统里其的作用与感光无关(Senthilan等,2012),可能演化过程中,其作用也不一定是从感光开始的。生物有很多奥秘,即使在分子层面也不一定就一时能完全清楚。
分子层面并非色觉研究的终点,大脑对色觉的理解还有更深、更多的机理,包括人类目前还不知道的奥秘。
注:
1. Kühne证明RPE参与视紫物质暗复原的实验:a.把青蛙的眼球置于光照之下30分钟,视网膜褪色,在黑暗中保存后紫色重现;b.褪色后的视网膜与RPE分离,在黑暗紫色不能复原;c.把褪色后的视网膜放在分离的RPE上,在黑暗中紫色可以复原;d.如果把c中的视网膜和RPE之间放置一片不通透的膜,不能复原;e.如果c中的RPE死亡时间过长(数小时),那么视网膜不能复原;f.如果漂白溶解在胆盐中的视紫物质,单独在黑暗中不能复原,而褪色的视紫物质如果与RPE混合则能在黑暗复原。
Kühne的遗嘱要求自己被火化时演奏贝多芬的第九交响乐(Ripps,2008)。
2. 本文将rhodopsin称为“视紫蛋白”。
3. 有关七重跨膜蛋白相关的部分内容也见“一个可能的诺贝尔化学奖”()
4. 牛顿《光学》出版于Hooke去世以后,与两人一直有争论可能有关。牛顿的名言“我如果看的远是因为站在巨人肩上(If I have seen further it is by standing on the should of giants)”出现于他与Hooke争论的通讯中,有两位英国传记作家解读可能是牛顿讽刺挖苦驼背的Hooke。不过,这句话并非牛顿发明,在十二世纪就有人提过。
5. George Wald与夫人Ruth Hubbard在1960、1970年代加入社会活动,如反核,但也曾错误地积极反对重组DNA,在1970年代导致哈佛所在地限制重组DNA的研究,有些教授逃跑,见。
6. Jeremy Nathans实验用了自己的所谓“种系发生细胞”是文雅地指精子。他的父亲为霍普金斯大学的Daniel Nathans(1928-1999),后者与研究生Kathleen Danna于1971年发现DNA了限制性内切酶。1973年美国旧金山加州大学(UCSF)生化系的Herbert Boyer和Stanford微生物系的Stanley Cohen在限制性内切酶的基础上,提出其后普遍通用的重组DNA方法,开创了基因工程的时代,奠定了生物技术产业的一个主要支柱,也改观了人类的生命科学研究。Daniel Nathans于1978年与瑞士的Werner Arber和美国的Hamilton Smith共享诺贝尔生理或医学奖。
参考文献:
Arshavsky VY, Lamb TD, Pugh Jr EN (2002) G proteins and phototransduction. Annual Review of Physiology 64: 153-187.
Baylor DA, Lamb TD and Yau KW (1979) Responses of retinal rods to single photons.Journal of Physiology 288:613-634.
Belrhali H, Nollert P, Royant A, Menzel C, Rosenbusch JP, Landau EM and Pebay-Peyroula E (1999). Protein, lipid and water organization in bacteriorhodopsin crystals: a molecular view of the purple membrane at 1.9 Å resolution. Structure 7:909-917.
Berson DM, Dunn FA and Takao M (2002). Phototransduction by retinal ganglion cells that set the circadian clock. Science 295:1070-1073.
Böll F (1877) Zur Anatomie und Physiologie der Retina. Arch. Anat. Physiol. Physiol. Abt:4-35.
Dalton J (1798). Extraordinary facts relating to the vision of colours with observations. Memoirs of the Literary and Philosophical Society of Manchester. 5:28-45.
Dowling JE(2002)George Wald 18 November 1906-12 April 1997. Proceedings of the American Philosophical Society 146:431-439.
Fesenko, E. E., Kolesnikov, S. S., and Lyubarsky, A. L. (1985) Induction by cyclic GMP of cationic conductance in plasma membrane of retinal rod outer segment. Nature 313:310 –313.
Fridericia LS and Holm E (1925). Experimental contribution to the study of the relation between night blindness and malnutrition. American Journal of Physiology 73:63–78.
Hargrave PA, McDowell JH, Sremiatkowski-Juszczak EC, Fong S-L, Kuhn H, Wang JK, Curtis DR, Mohana Rao JK, Argos P, and Feldmann RJ (1982). The carboxy terminal one-third of bovine rhodopsin: its structure and function. Vision Research 22:1429-1438.
Hargrave P. A., McDowell J. H., Curtis D. R., Wang J. K., Juszczak E., Fong S. L., Rao J. K., Argos P. (1983) The structure of bovine rhodopsin. Biophysics of Structure and Mechanism 9:235–244.
Hattar S, Liao HW, Takao M, Berson DM and Yau KW (2002). Melanopsin containing retinal ganglion cells: architecture, projections, and intrinsic 295:1065-1070.
Hecht S (1919). Sensory equilibrium and dark adaptation in Mya arenaria.Journal of General Physiology i(5):545-58.
Hecht S, Shlaer S, Pirenne M (1942) Energy, quanta and vision. Journal of General Physiology 25:819–840.
von Helmholtz H (1910) Treatise on Physiological Optics, translated by Southall JPC (1924), Vol. 2 the sensations of vision. The Optical Society of America.
Horiguchi H, Winawer J, Dougherty RF, Wandell BA (2012). Human trichromacy revisited. Proceedings of the National Academy of Sciences USA 110:260-269.
Hunt DM, Dulai KS, Bowmaker JK, Mollon JD (1995). The chemistry of John Dalton’s color blindness. Science 267:984 – 988.
Kimura, Y., Vassylyev, D.G., Miyazawa, A., Kidera, A., Matsushima, M., Mitsuoka, K., Murate, K., Hirai, T. & Fujiyoshi, Y. (1997). Surface of bacteriorhodopsin revealed by high-resolution electron crystallography. Nature 389:206-211.
Kühne W. (1879) Chemische Vorgänge in der Netzhaut. Hermann L. eds. Handbuch d. Physiologie d. Sinnesorgane Erster Theil, Gesichtssinn. F.C.W. Vogel Leipzig, Germany.
Kühne W (1882). Beiträge zur Optochemie. Untersuchungen aus dem physiologischen Institute der Universität Heidelberg 4:169-249.
Marks WB, Dobelle WH, MacNichol EF (1964) Visual pigments of single primate cones. Science 143:1181-1183.
Maxwell JC (1872). On colour vision. Proceedings of the Royal Institution of Great Britain 6:260-271.
McCollum, E. V. and Davis, M. (1913) The necessity of certain lipins in the diet during growth. Journal of Biological Chemistry 15:167–175.
McCollum, E. V. and Davis, M. (1915) The nature of the dietary deficiencies of rice. Journal of Biological Chemistry 23:181–230.
Müller R (1851). Zur Histologie der Netzhaut. Z. Wiss. Zool. 3:234-237.
Nathans J and Hogness DS (1983) Isolation, sequence analysis, and intron-exon arrangement of the gene encoding bovine rhodopsin Cell 34:807-814.
Nathans J and Hogness DS (1984) Isolation and nucleotide sequence of the gene encoding human rhodopsin. Proceedings of the National Academy of Sciences USA 81:4851-4855.
Nathans J, Thomas D, Hogness DS (1986). Molecular genetics of human color vision: the genes encoding blue, green, and red pigments. Science 232:193-202.
Nathans J, Piantanida TP, Eddy RL, Shows TB and Hogness DS (1986). Molecular genetics of inherited variation in human color vision. Science 232:203-210.
Newton I (1704). Opticks.
Osborne TB and Mendel LB (1913) The relation of growth to the chemical constituents of the diet. Journal of Biological Chemistry 15:311-326.
Ovchinnikov Iu A., Abdulaev N. G., Feigina M., Artamonov I. D., Bogachuk A. S.(1983) Visual rhodopsin. III. Complete amino acid sequence and topography in a membrane. Bioorganicheskaia Khimiia 9:1331–1340.
Palczewski K., Kumasaka T., Hori T., Behnke C. A., Motoshima H., Fox B. A., Le Trong I., Teller D. C., Okada T., Stenkamp R. E., Yamamoto M., Miyano M.(2000) Crystal structure of rhodopsin: a G protein-coupled receptor. Science 289:739–745.
Palmer, G. 1777a. Theory of Colour and Vision, London: Leacroft.
Palmer, G. 1777b. Theorie du couleur et de la vision, translated by D.-B. Quatremere d'Isjonval, Paris: Pissot.
Provencio I, Jiang G, De Grip WJ, Hayes WP, Rollag MD (1998) Melanopsin: an opsin in melanophores, brain, and eye.Proceedings of the National Academy of Sciences USA 95:340–345.
Provencio I, Rodriguez IR, Jiang G, Hayes WP, Moreira EF and Rollag MD (2000) A novel human opsin in the inner retina. Journal of Neuroscience 20:600-605.
Ripps H (2008). The color purple: milestones in photochemistry. FASEB Journal 22:4038-4043.
Senthilan PR, Piepenbrock D, Ovezmyradov G, Nadrowski B, Bechstedt S, Pauls S, Winkler M, Möbius W, Howard J, Göpfert MC (2012).Drosophila auditory organ genes and genetic hearing defects. Cell 150:1042-1054.
Smith SO (2010). Structure and activation of the visual pigment rhodopsin annual review of biophysics. Annual Review of Biophysics 39:309-328.
van der Velden HA (1946) The number of quanta necessary for the perception of light in the human eye. Opthalmologica 111:321–331.
Wald G (1933)Vitamin A in the retina. Nature 132:316.
Wald G (1935) Vitamine A in eye tissue. Journal of General Physiology 18 :905-915.
Wald G (1935) Carotenoids and the visual cycle. Journal of General Physiology 19:351-371.
Wald G. (1968). The molecular basis of visual excitation. Nature 219:800-807.
Wolf G (2001). The discovery of the visual function of Vitamin A. Journal of Nutrition 131:1647-1650.
Young T (1802) On the Theory of Light and Colours. Philosophical Transactions of the Royal Society of London 92:12-48.
Yudkin AM (1931) The presence of vitamin A in the retina. Archive of Ophthalmology 6:510–517.
写于2011年4月
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 