阅读:0
听报道
2012年2月7日,犹太裔意大利生物学家蕾塔·列维-芒塔齐尼(Rita Levi-Montalcini,1909-)发表最新研究论文。她于1986年获诺贝尔生理学奖,2009年4月22日成为第一位诺贝尔百岁寿星。所以,刚刚在《美国科学院院刊》发表新论文的她接近103岁高龄。

无独有偶,她曾经的合作者、犹太德裔美国生物学家汉伯格(Viktor Hamburger,1900-2001),也颇长寿并在99岁还发表文章。
在科学贡献上,他们是二十世纪后五十年最重要的两位发育神经生物学家,而前五十年是德国的Hans Spemann和美国的Ross G Harrison。
蕾塔·列维-芒塔齐尼作为孪生女出生于意大利Turin,读Turin大学医学院的同学还有两位诺贝尔奖得主:Renato Dulbecco(1914-)和犹太裔的Salvador Luria(1912-1991)。他们在Turin的导师是Giuseppe Levi。
二战期间,法西斯统治的意大利使犹太血统的蕾塔失学、失业,她就在家做实验。二战后的1947年,她到美国密苏里州的圣路易斯市,在华盛顿大学动物系(后称生物系)工作,做出重要发现,将近三十年后才回意大利。
蕾塔发现神经生长因子(nerve growth factor, NGF),不仅对于神经发育很重要,也是第一个细胞生长因子。她一辈子扑在NGF上,2012年发表的论文还是研究NGF。
汉伯格1920年代的研究生导师是德国胚胎学家、第一位发育生物学的诺贝尔奖得主Spemann。1932年汉伯格获洛克菲勒基金会资助到芝加哥大学合作研究,1933年德国通知他因为是犹太人而被除名,Spemann也来信告知爱莫能助。幸亏洛克菲勒基金会很快建立了紧急基金来支持被纳粹除名的科学家。汉伯格在芝加哥大学工作两年后,南迁密苏里州的圣路易斯市,加入华盛顿大学,1941年任动物系主任,1989年获国家科学奖。
蕾塔一生相当专注于研究NGF,而汉伯格有多方面工作。他将德国的胚胎学传统带到美国,多年为神经胚胎学的领袖。他研究出色,还积极教学,写书,发挥了智力领导的作用,他的影响以及蕾塔·列维-芒塔齐尼的研究,使华盛顿大学长期为世界发育神经生物学的重镇。八十年代全世界学习发育神经生物学的教科书大多采用华盛顿大学Dale Purves和Jeff Lichtman编的《神经发育原理》。汉伯格除原创性研究,还做自己领域需要的描述性基础工作,例如他和Hamilton于1951年确定鸡胚分期的工作,虽非创造性研究,但非常实用,该文被引用已过万次,并不断有人继续引用。
细胞死亡和细胞生存
有很长时期,研究细胞的科学家只关注生长,而不注重死亡,以为死亡无需机制。很多细胞生物学家误认为1970年代才发现细胞死亡,其实那是对细胞凋亡的描述和定义,而细胞死亡几十年前在神经系统就发现了。法国细胞学家Collin(1906)在题为“神经细胞发育的细胞学研究”一文中,已经注意到6日鸡胚中有细胞死亡,但并未意识到其重要性。1920到1930年代,德国海德堡大学Kallius指导的学生Ernst(1926)和Glücksmann(1930)研究高等动物中细胞死亡,他们进行了仔细观察,并将细胞死亡分类,他们明确地知道,在发育过程中,多处出现细胞死亡。
细胞死亡是否被调节?这个问题起源于研究肢体和神经的关系。功能上,肢体是神经所支配的靶组织,其中两种神经纤维,位于背根神经节的感觉神经细胞送出感觉神经纤维到达肢体、将肢体的感觉信息传入神经系统;位于脊髓腹角的运动神经细胞送出运动神经纤维到达肢体、将神经系统的指令传出到肢体指挥其运动。神经对肢体的支配发生在胚胎发育过程中,早期肢体刚开始发育时称为肢芽、或原基。
芝加哥大学Lillie实验室的研究生Shorey(1909)在鸡胚发现,电损毁前肢(翅膀)的芽盘后,支配它的感觉神经节和运动神经中心都减小。耶鲁大学的研究生Detwiler(1920)用蝾螈发现,如果将前肢的原基去除,支配它的感觉神经节减小,而如果通过移植在胚胎一侧多加一个前肢原基,支配的感觉神经节也会增大。汉伯格1932年到Lillie实验室后重新捡起Shorey的实验,1934年他发表文章确定可以重复Shorey的结果,缺失靶组织后,导致支配它的感觉和运动神经中心减小。1939年他发表文章,说明用鸡胚重复了Detwiler的实验,发现实验增加靶组织会增大支配它的感觉和运动中心。这些研究显示:靶组织调节神经的发育,使支配的神经和靶组织之间相匹配。
为什么神经与其外周靶组织会匹配?Detwiler提出靶组织调节神经细胞的分裂和增殖,汉伯格提出靶组织发出的信号,来影响未分化的神经细胞进行分化。1944年汉伯格和Keefe实验证明,细胞增殖并不参与此过程。
汉伯格将1934的文章的单行本寄给意大利的Levi教授。Levi将论文给了学生蕾塔·列维-芒塔齐尼。蕾塔于1981年回顾:“那是墨索里尼对法宣战的1940年6月,有一天我在送牛的火车箱地板上,读Viktor的文章”。Cattle coach是用于运送动物的货车车厢,有时用来载人,失业的蕾塔在牛车上也急于了解科学发现。
蕾塔虽然看重汉伯格的结果,但不同意其解释。她没有实验室,就在卧室做研究,到菜市买鸡蛋,做完实验把剩下的鸡蛋吃了。她和Levi的文章发表于1942的《比利时生物学志》。她重复了汉伯格的实验,但更仔细地分析了神经节内的神经细胞数量。她看到,在胚胎发育的特定几天,未分化的神经细胞数量随发育而减少,因为分化了而长出神经纤维的神经细胞数量在同一阶段增加。她发现,如果去除鸡胚一侧后肢的肢芽,未分化的神经细胞数量不受影响(等同于未去除肢芽的一侧),而分化的神经细胞数量逐渐减少。她认为这些结果提示:去除肢芽不影响神经细胞的分裂和分化,而影响神经细胞的生存。
战后,汉伯格读到蕾塔和Levi的文章,1946年他邀请蕾塔来他实验室,不同意见的研究者开始合作。1947年秋天蕾塔到圣路易斯计划做半年实验,结果待了近三十年。1949年,汉伯格与蕾塔·列维-芒塔齐尼合作发表论文,实验是蕾塔做的,分析的是她熟悉的感觉神经节。该研究不仅通过染色可以看到细胞蜕变,证实1942和1944年她的解释是对的,而且发现,在正常发育过程中,自然出现大量的细胞死亡。他们也看到,细胞死亡发生在神经纤维已经长到靶组织的时候。他们提出,去除靶组织导致支配的神经细胞的蜕变,而在正常发育过程中,纤维长到靶组织的神经细胞数量多于靶组织的需要,过多的神经细胞得不到靶组织环境的条件而死亡。同年开会时,汉伯格和蕾塔(1950)用了营养性(trophic)一词,说明靶组织对神经细胞的作用。
至此,确立了几个概念:发育过程中自然发生细胞死亡、靶组织对神经细胞生存的影响、细胞间的营养性作用。
以上工作,汉伯格和蕾塔·列维-芒塔齐尼都起了重要作用。之前,虽然1909和1920年有过实验、但问题的重要性未被认识,汉伯格在1934年后积极推动,确立现象后力图建立概念。而蕾塔·列维-芒塔齐尼首先得到正确的解释,他们合作建立了多个新概念。
神经生长因子
神经生长因子的研究,蕾塔·列维-芒塔齐尼的工作多于汉伯格。
不过,1939年,汉伯格就曾提出:“外周产生控制生长的因子(growth controlling agent),向心性传到运动中心”。这个概念,等于是神经生长因子的影子。但这并非他当时唯一的解释,他和蕾塔1949年文章还提出过两种解释,其中第二个解释与此类似。
汉伯格以前的一个研究生Elmer Bueker(1943,1945)一边打工养家一边做研究生论文,他重复汉伯格的肢芽移植实验,结果相同。1948年,已到外地任教的Bueker别出心裁,把肿瘤移植到鸡胚,他想看,生长快的肿瘤能否影响神经细胞的生长。他首先用小鼠乳腺腺细胞肉瘤(肉瘤180)和Rous禽肉瘤,结果发现移植Rous禽肉瘤的鸡胚都死了,移植肉瘤180的鸡胚常常把肉瘤给吸收了。但是,在没有被吸收的几例中,肉瘤得到了神经支配,而且支配它的感觉神经节体积大于正常。
蕾塔和汉伯格曾试图找可以影响神经细胞生长的组织,发现脑、肝、肌肉和皮肤都不行。汉伯格于1948年秋给蕾塔看Bueker的文章,蕾塔看后决定也做肉瘤。汉伯格写信给Bueker征求他同意重复和扩充其研究,然后从Jackson实验站要了四种肉瘤,肉瘤180以外,还有肉瘤37以及另外两种乳腺瘤。蕾塔重复了Bueker的实验,也移植过老鼠胎盘,结果肉瘤180和37能增加感觉神经节细胞的分裂、分化和生长,老鼠胎盘对鸡胚无此作用。肉瘤的作用不依赖于神经纤维和肉瘤细胞建立突触连接,这些结果由Levi-Montalcini和Hamburger在1951年发表。蕾塔觉得可能有弥散性物质参与此过程,就把肉瘤移植到其它远离神经的地方,结果也有作用,这些发现,她先单独在会议宣读、在会议集发表(1952),1953年与汉伯格共同正式发表。
蕾塔曾试图检验肉瘤的提取物能否有同样作用,没成。然后她想做体外实验。她联系了自己的意大利朋友、当时在巴西工作的Herta Meyer,后者会做体外培养。汉伯格为蕾塔安排洛克菲勒基金会的资助,蕾塔于1952年9月揣了两只移植了肉瘤的老鼠飞到里约热内卢,她把感觉神经节放到体外培养,然后加入小片肉瘤,她把结果画成图寄给汉伯格。1953年1月她回圣路易斯继续同类实验。1954年她和Meyer、汉伯格报道,在体外培养中,她们发现肉瘤180和37在十几、二十小时就可以增加神经节长出很多神经纤维。另外几种瘤没有这样的作用。有作用的肿瘤细胞,只要和神经细胞共培养就行,无需直接接触,说明肉瘤细胞分泌可弥散的分子作用于神经细胞。
如何拿到这种可弥散的分子?蕾塔和汉伯格都没有分离纯化的技术专长。但是,和校本部相隔一个“森林公园”的医学院有。1940和1950年代,正是华盛顿大学生物化学的鼎盛时期。生物化学系以Carl和Gerty Cori夫妇(1947年诺贝尔奖,研究糖原代谢)为首,他们两人实验室出了8位诺贝尔奖获得者,而微生物系也是生化学家领导,系主任是犹太裔Arthur Kornberg(1918-2007,1959年诺贝尔奖,发现DNA多聚酶)。他们在华盛顿大学医学院的基础和临床系科形成了很强的生化圈。通过熟悉生化圈,汉伯格邀请在放射科做博士后的犹太裔生化学家Stanley Cohen(1922-)到校本部汉伯格自己主持的动物系,加入寻找生长因子的研究。雇到Cohen时,蕾塔还在巴西,她回信给汉伯格说“从你的描述看来,他是着手从事发现肉瘤释放分子这样困难问题的正确人选”。
Cohen熟悉生物化学技术,他加入后分离纯化因子的进展很快。1954年,Cohen、Levi-Montalcini和Hamburger通过汉伯格投稿《美国科学院院刊》,报道他们将肉瘤细胞破碎成匀浆,仍可检测到活性,刺激感觉神经细胞长出神经纤维。活性组分在当时未完全分离纯化的情况下,还含核酸和蛋白质,加热可以失活。他们论文的题目是“肉瘤37和180中的神经生长刺激因子”。
此后,汉伯格淡出神经生长因子的研究,蕾塔·列维-芒塔齐尼和Cohen继续。
Cohen不仅在校本部做神经发育的实验,而且经常穿过公园到医学院参加生物化学的学术活动。当时,Kornberg主持的微生物系每天中午有学术报告和午餐,听众中不仅有当时的生物化学大家、也有以后成名的分子生物学大家,如Paul Berg(1980诺贝尔奖)、David Hogness、Dale Kaiser,以后都被Kornberg带到斯坦福大学建立生化系。Cohen在微生物系的学术活动中讲了自己的结果,Kornberg说你这是在研究病毒,如果是病毒,里面就有核酸,Kornberg建议Cohen用磷酸二酯酶降解病毒的核酸,来证明是否确有病毒参与。微生物系日裔助理教授早石修(Osamu Hayaishi,1986年Wolf奖得主)用一种蛇毒制备了磷酸二酯酶的粗提物。Cohen和蕾塔赶紧用它做了实验,结果发现,不仅肉瘤的活性没有下降,而蛇毒制备物本身就有很强的活性,反而刺激了神经纤维的生长。原因是这种粗提物不是很纯,不仅有磷酸二酯酶,而且还有生长因子。Cohen和蕾塔1956年发表论文“蛇毒中的神经生长刺激因子”。1957年,他们有更多证据提示此因子是蛋白质,包括它对热敏感、对多种蛋白酶敏感。1960年,Cohen报道小鼠唾液腺中也有神经生长促进作用,用多种方法分离纯化后活性更高,分子量估计4万4千道尔顿,文内用了“神经生长因子”一词。NGF的活性不仅对热敏感、而且可以被蛋白酶所降解。Cohen制备了NGF的抗体,而注射此抗体到新生或成年小鼠体内后,可以破坏交感神经系统。同期杂志中,Levi-Montalcini与Booker发表一篇文章报道Cohen提取的因子也刺激体外培养的人胚胎交感神经节,如果注射到新生或者成年小鼠,也刺激体内交感神经节生长。她们还发表一篇文章,发现注射因子的抗体后,小鼠、大鼠、兔、猫、猴的交感神经都大大减小,仔细分析了其中变化。所以,体外和体内实验证明因子可以促进神经生长,而用功能阻断的抗体可以破坏体内已经生长的神经,证明其对神经维持的必要性。
Cohen的以上工作都在华盛顿大学进行,发表时他已到Vanderbilt大学任助理教授,因为汉伯格系里缺乏经费留Cohen任教。此后,Cohen研究NGF不多,而主要集中研究表皮生长因子EGF。
1960年代,几个实验室试图确定纯化的NGF蛋白质的氨基酸序列,1971年,Angeletti和Bradshaw确定了NGF是由118个氨基酸组成的蛋白质,分子量为13250道尔顿。
汉伯格在1970和1980年代,重新回到神经细胞死亡的研究,他和其他人证明神经生长因子可以抑制正常发育过程中出现的神经细胞死亡。
研究的长处和短处
汉伯格、Levi-Montalcini、Cohen以及后继者,从1950年代初期到1971年寻找NGF的过程,很重要的长处是他们开创一个领域。
在50年代的研究中,他们建立了比较方便的体外实验,也一直注意做体内实验。拿到NGF以后,不仅确定其能对神经细胞发生作用,而且很快就制备了抑制其功能的抗体,而注射抗体可以破坏体内神经系统,证明NGF、或有NGF样免疫特征(对所制备抗体有反应)的分子在体内参与维持神经系统,两套实验分别验证了充分性和必要性。
我们复习的50和60年代工作,也有不足之处。他们在做实验过程中换了生长因子来源的靶组织,从最初的肢芽,到肉瘤和唾液腺。那么有可能,这些不同的组织和细胞含不同因子,肉瘤和唾液的分子可能完全不同于肢芽的分子。
用来检测的神经组织也有变化,开始做鸡胚实验是检测感觉神经节中的感觉神经元和脊髓腹角的运动神经元,后来常用交感神经节中的交感神经元。
在检测过程中,他们做过不同的细胞生物学现象,如分裂、分化和死亡。而很有可能,某个分子只有一个作用,而不是所有作用,如果一定要找抑制死亡的分子,那么就要坚持检测死亡,而不是看到长了很多神经纤维就算有活性。刺激神经纤维的生长,可能是细胞分裂多了,也可能是细胞分化多了所以长出很多纤维,也可能是细胞死亡少了。Levi-Montalcini和Cohen在研究过程中,有时注意了用多种检测,有时没有,因为有些检测很快就很方便地得到很强的结果。
用抗体做的实验,为了操作方便,注射到新生和成年小鼠,而用鸡胚做的实验用的发育阶段远远早于1960年抗体实验用的阶段,完全可能NGF只参与早期的发育,而不参与出生后的发育和维持。开始不易用胚胎做抗体注射的实验,以后得到改善,当然最清晰的实验需要等有基因剔除技术后。
既然他们没有找到解释最初活性的分子,而还有其它一些问题,那么,为什么还是公认他们做出了重要的贡献?
最重要的是,当时很少人研究细胞分裂、分化和死亡,他们无论得到影响其中哪一个现象的分子,都是重要的,这是不做热门而开辟一个领域的好处,如果是在一个研究人员很拥挤的领域,混淆这些问题就不容易进展。
另外,后来知道NGF本身有多种作用。比如,NGF可以刺激神经细胞分化长出神经纤维,这个作用与细胞死亡的作用是分开的,有些其他分子只有刺激分化的作用,不能抑制死亡。NGF两个作用都有。直到1970和1980年代,才有更好的实验证明纯化的NGF直接抑制细胞死亡,而不是通过增加细胞分离、或细胞分化。
40年代起初的观察是肢芽对感觉神经元和运动神经元的作用。60和70年代找到的NGF不能解释肢芽的作用,至少不能解释肢芽的全部作用,因为虽然NGF对背根神经节的感觉神经元有营养性作用,NGF对运动神经元没有营养作用。后来发现的其它神经营养性因子及其它生长因子,对运动神经元有营养性作用。现在还有人认为肢芽(和作为靶组织的肌肉细胞)含有其它未知分子,尚需研究。
基础和应用的曲折关系:无心插柳柳成荫
这些工作,都是基础研究,起初没有应用目的。1980年代以后有很多人尝试,神经营养性因子对疾病中的细胞蜕变是否有治疗效果,目前还没有上临床。
但是,另外一个研究却和应用关系很大。不过,也非当初目的,且无可预见。就是表皮生长因子EGF的研究。
Cohen在离开华盛顿大学以前,偶然发现小鼠颌下腺有生物活性,可以提前让新生小鼠眼睛睁开。他到Vanderbilt大学后继续此项研究,1962年发表第一篇文章,以后纯化此分子,更进一步确定其生物活性,1965年,他命名为EGF。对EGF的研究,特别是其受体的研究,建立了受体磷酸酶的典型。EGF的工作起初只与发育有关,后来其他人发现与肿瘤有关,EGF的受体基因突变后,可以造成肿瘤,其机理相似于Rous肉瘤产生的原理:都是因为蛋白激酶活性过高造成。
二十年后发明针对EGF受体的药物,EGF受体选择性拮抗剂,是通过分子机理来进行合理药物设计的典范,成为今天抗肿瘤的常用药物。比较可笑的是,Cohen和蕾塔当初用肉瘤做NGF,最后却与肿瘤关系很小,而Cohen用老鼠睁开眼皮的实验,却与肿瘤关系很大,不过不是眼皮的癌症,而是肺癌等其他常见癌症。
相关的几个药物给药厂每年带来上十亿美元的销售,而它们更是救了很多病人的命。
生物学研究中,不很容易从最初用的材料来确定是否将来有实用价值。
越走越宽
1982年,德国的Barde和Thoenen发现脑中神经营养性因子活性BDNF,并于1989年获得其基因,BDNF和NGF是同一个家族,结束了NGF孤单的历史,此后很快多个实验室用分子生物学技术找到多个神经营养性因子,他们分别和协同对不同神经细胞起营养性作用。
NGF是如何起作用的?1986年,美国的Moses Chao获得第一个NGF受体的基因,此受体现在一般称为p75。1991年,两个实验室发现Trk癌基因编码的蛋白激酶也是NGF的受体。Trk与p75有协同有分工,三个Trk分别参与将细胞外不同的神经营养性因子的信号转导到细胞内。
从此,很多人加入研究神经营养性因子的领域,发现更多有趣的特性和功能,比如这些蛋白质从前体加工而来、但“前体”有不同于成熟蛋白质的功能。神经营养性因子的作用,也不止神经细胞的生长和存活…。蕾塔2012年的文章报道用NGF的抗体注射到早期鸡胚后,胚胎的轴转向受到影响,这是早于神经发育的一个步骤。
神经营养性因子,最初十几年是只有几个人做的课题,现在是成百上千神经生物学研究者的领域。而发现细胞的生长因子,有更广泛的意义,存在于针对多种细胞的不同生长因子,除了NGF、EGF,还有FGF、TGFb、PDGF、VEGF…遍布生物医学很多领域,而且作用很重要,现在可能上万人的研究和生长因子有关。
无论生长因子、还是神经营养性因子,目前都有很多活跃的研究。
诺贝尔奖委员会惹的祸
1986年以前,汉伯格和蕾塔·列维-芒塔齐尼关系很好,他们单独写文章回忆的时候都肯定对方,到1980年代初两人分别发表的论文都标明过“献给”对方。1986年,诺贝尔生理或医学奖给蕾塔·列维-芒塔齐尼和Cohen,而无汉伯格,带来不良反应。
虽然蕾塔在自己的诺贝尔奖演说中明确注释:“本文献给促进和参与本研究的Viktor Hamburger,我永远感激他无价的提示和慷慨。没有他,神经生长因子永远不会得到我们的注意”,但是他们的关系因为委员会的决定和他们两人其后对记者谈话出现很大裂痕。
华盛顿大学出产的多个发育神经生物学的权威,如Max Cowan、Dale Purves,以及那时正在上升的Josh Sanes等,都曾公开发表文章,不满诺贝尔奖委员会的决定。
在1940和1950年代女性科学家比较受歧视的情况下,汉伯格比较突出地支持蕾塔·列维-芒塔齐尼。同在华盛顿大学的犹太裔捷克女生化学家Gerty Cory(1896-1957),做了很多年的非正规教职,到她得诺贝尔奖后的1948年才正式成为教授。华盛顿大学是全世界极少数出产两位女性诺贝尔科学奖得主的大学之一,其对待女性有问题,那么其他学校问题就更大。而汉伯格对待蕾塔,与整体环境形成了鲜明对照。他请她从意大利来美国,不仅合作、而且支持她独立的工作,帮她雇Cohen来做分离纯化,支持她在1958成为正教授。在这样的背景下,更容易理解为什么汉伯格不满她得奖后对媒体的回答,不和她说话、拒见回访华盛顿大学的她。1992年,汉伯格撰文介绍细胞死亡概念的来由。
一个本来美好的关系,被诺贝尔奖委员会破坏了。
有趣的是,汉伯格的女婿得了诺贝尔奖,不过很多人认为其工作不该得奖,是诺贝尔奖委员会的另外一种错误。
汉伯格和列维-芒塔齐尼对我和朋友的影响
1985年,我和鲁白离开上海第一医学院同一个教研室和同一个寝室到美国念研究生。在国内我们已开始念神经生物学,但非发育神经生物学,而到美国不久都很快转成发育神经生物学。我到UCSF听了很多激动人心的发育生物学学术报告而转向。鲁白在Cornell医学院的实验室当时主要研究NGF,1986年诺贝尔奖给NGF工作,我挑战性地问过鲁白是否还有重要工作可做,他认为有。事实上他不仅研究生期间做NGF,以后一直研究NGF及其他神经营养性因子,特别是对BDNF参与神经可塑性、甚至人类记忆的关系也有研究,超出当初单纯的胚胎发育范围。他还希望推动用神经营养性因子治疗疾病。
1994年我到华盛顿大学工作后,与Jeff Lichtman去汉伯格家。那时他已退休多年,但仍写很多科学史的文章,特别是用他自己的背景介绍了一些后来人不知道和不懂的历史工作,包括现在很多人不能读的德文文献。我很喜欢看汉伯格的书,并直接影响了我实验室的研究。他写过一本回顾Spemann的书,其中介绍有时超出Spemann本人的研究。我实验室偶然发现一个基因ET在胚胎早期表达在眼睛里面。此前,我没研究过眼睛,看到ET表达在两个眼睛里面,很漂亮,再一看,好像更早期的时候,ET表达是一个眼睛连续到另外一个眼睛成为一条带,这条带在发育过一段时间后,中间段ET表达下降,而只剩下表达在两边眼睛。这个表达型式,突然使我想起汉伯格书里讲过1936年以前的一些研究,那是几十年前科学家争论两个眼睛是怎么起源的,是分开起源,还是本来在一起后来分开。我实验室(特别是李华顺)从这条线索开始,做了一系列研究,证明两个眼睛来源于同一前体,一分为二是因胚胎的中胚层送出一个信号给眼睛所在的外胚层所致,如果去除中胚层,这条带就不能分开而成为一个大大的眼睛,这些结果于1997年发表,其后多个实验室的结果看来,此机理在可能普遍存在于哺乳动物。在我们文章发表以前,我和李华顺去了96岁的汉伯格家,他对六十年前其他实验室的研究结果如数家珍。
汉伯格于2001去世,是我在美国唯一参加的葬礼。
愿蕾塔·列维-芒塔齐尼继续发表新发现。

图片说明
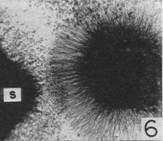
图一为1977年Viktor Hamburger和Rita Levi-Montalcini,由Rita Levi-Montalcini(1982)发表。
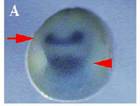
图二显示肉瘤(图片左边)刺激下,鸡胚的感觉神经节(右边)生长大量神经纤维,来自Cohen, Levi-Montalcini, Hamburger (1954)。同一文章还有图显示肉瘤的提取物也有同样活性。
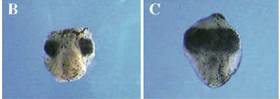
图三A部分是ET基因在蛙胚胎发育早期的表达,上面一条线从左眼前体连接到右眼前体,F部分显示发育稍后同样ET的表达只在两侧眼睛,中间区域没有。
图四B部分是蝌蚪在有中胚层信号的情况下,长出两个眼睛,C部分是当去除中胚层后,两个眼睛连续成一块。图三和四来自Li HS, Tierney C, Wen L, Wu JY and Rao Y (1997). A single morphogenetic field gives rise to two retina primordia under the influence of the prechordal mesoderm. Development 124:603-615。
读物
I 回顾与综述
Levi-Montalcini R, Angeletti PU (1968). Nerve growth factor. Physiol Rev 48:534-569.
Levi-Montalcini R. 1982. Developmental neurobiology and the natural history of nerve growth factor. Annu Rev Neurosci 5:341–62.
Levi-Montalcini R (1987) Nerve growth factor 35 years later. Science 237:1154-1162.
Purves D & Sanes JR (1987) The 1986 Nobel Prize in physiology or medicine. Trends Neurosci 10:231–35.
Levi-Montalcini R (1988) In Praise of Imperfection: My Life and Work. Basic Books, New York.
Oppenheim RW (1991) Viktor Hamburger (1900–2001). Neuron 31:179-190.
Hamburger V (1992) History of the discovery of neuronal death in embryos. J Neurobiol 23:1116-1123.
Cowan WM (2001) Viktor Hamburger and Rita Levi-Montalcini: the path of discovery of nerve growth factor. Annu Rev Neurosci 24:551–600
Cohen S (2008) Origins of growth factors: NGF and EGF. J Biol Chem 283:33793–33797.
Abbot A (2009). One hundred years of Rita. Nature 458:564-567.
II 原始论文
从靶组织对支配神经的作用到细胞死亡
Collin R (1906). Recherches cytologiques sur le developpement de la cellule nerveuse. Névruxe 8:181-308.
Ernst M. (1926). Über Untergang von Zellen während der normalen Entwicklung bei Wirbeltieren. Z Anat Entwickl 79:228-262.
Glücksmann A (1930). Ueber die Bedeutung von Zellvorgngen fur die Formbildung epithelialer Organe. Zeitschr Anat u Entw gesch 93:35-92.
Shorey M (1909). The effect of the destruction of peripheral areas on the differentiation of the neuroblasts. J Exp Zool 1:25-64.
Detwiler S (1920). On the hyperplasia of nerve centers resulting from excessive peripheral loading. Proc Natl Acad Sci 6:96-101.
Hamburger V (1934). The effects of wing bud extirpation on the development of the central nervous system in chick embryos. J Exp Zool 68:449-494.
Hamburger V (1939). Motor and sensory hyperplasia following limb-bud transplantations in chick embryos. Physiol Zool 12:258-284.
Levi-Montalcini R & Levi G (1942). Les conséquences de la destruction d'un territoire d'innervation périphérique sur le développement des centres nerveux correspondants dans l'embryon de poulet. Arch Biol Liège 53:537-545
Hamburger V & Keefee L (1944) The effects of peripheral factors on the proliferation and differentiation in the spinal cord of chick embryos. J Exp Zool 96:223-242.
Levi-Montalcini R & Levi G (1944). Correleziani nello svillugo tra varie parti del sistema nervoso. I. Consequenze della demolizione delle abbozzo di un arts sui centri nervosi nell' embrione di pollo. Comment Pontif Acad Sci 8:527–568.
Hamburger V & Levi-Montalcini R (1949). Proliferation, differentiation and degeneration in the spinal ganglia of the chick embryo under normal and experimental conditions. J Exp Zool 111:457-502.
Hamburger V & Levi-Montalcini R (1950). Some aspects of neuroembryology. neuroembryology. In: Genetic Neurology. P. Weiss, Ed. University of Chicago Press, Chicago, IL, pp. 125-160.
寻找NGF
Bueker ED (1943). Intracentral and peripheral factors in the differentiation of motor neurons in transplanted lumbosacral spinal cords of chick embryos. J Exp Zool 93:99–129.
Bueker ED (1945). The influence of a growing limb on the differentiation of somatic motor neurons in transplanted avian spinal cord segments. J Comp Neurol 82:335–61.
Bueker ED (1948). Implantation of tumors in the hind limb field of the embryonic chick and the developmental response of the lumbosacral nervous system. Anat Rec 102:369–90.
Levi-Montalcini R, Hamburger V (1951). Selective growth stimulating effects of mouse sarcoma on the sensory and sympathetic nervous system of the chick embryo. J Exp Zool 116:321–61
Levi-Montalcini R (1952) Effects of mouse tumor transplantation on the nervous system. Ann N Y Acad Sci 55:330–344
Levi-Montalcini R, Hamburger V (1953). A diffusible agent of mouse sarcoma producing hyperplasia of sympathetic ganglia and hyperneurotization of viscera in the chick embyro. J Exp Zool 123:233–287.
Levi-Montalcini R, Meyer H, Hamburger V (1954). In vitro experiments on the effects of mouse sarcomas 180 and 37 on the spinal sympathetic ganglia of the chick embryo. Cancer Res 14:49–57.
Cohen S, Levi-Montalcini R, Hamburger V (1954). A nerve growth-stimulating factor isolated from sarcoma 37 and 180. Proc. Natl. Acad. Sci. USA 40:1014–18.
Cohen S, Levi-Montalcini R (1956). A nerve growth-stimulating factor isolated from snake venom. Proc Natl Acad Sci USA 42:571–74.
Cohen S, and Levi-Montalcini R (1957) Purification and properties of a nerve growth-promoting factor isolated from mouse sarcoma 180. Cancer Res 17:15–20.
Cohen S (1959) Purification and metabolic effects of a nerve growth-promoting protein from snake venom. J Biol Chem 234:1129–1137.
Cohen S (1960). Purification of a nerve-growth promoting protein from the mouse salivary gland and its neurotoxic antiserum. Proc Natl Acad Sci USA 46:302–11.
Levi-Montalcini R, Booker B (1960a). Excessive growth of the sympathetic ganglia evoked by a protein isolated from mouse salivary glands. Proc Natl Acad Sci USA 46:373–84.
Levi-Montalcini R, Booker B (1960b). Destruction of the sympathetic ganglia in mammals by an antiserum to a nerve growth protein. Proc Natl Acad Sci USA 46:384–91.
Cohen S (1962). Isolation of a mouse submaxillary gland protein accelerating incisor eruption and eyelid opening in the newborn animal. J Biol Chem 237:1535–62.
Angeletti RH, Bradshaw RA (1971). Nerve growth factor from mouse salivary gland: Amino acid sequence. Proc Natl Acad Sci USA 68:2417-20.
神经营养性因子家族及其受体
Barde YA, Edgar D, Thoenen H (1982). Purification of a new neurotrophic factor from mammalian brain. EMBO J 1:549-553.
Leibrock J, Lottspeich F, Hohn A, Hofer M, Hengerer B, Masiakowski P, Thoenen H, Barde Y-A (1989). Cloning and expression of brain-derived neurotrophic factor. Nature 341:149-152.
Johnson D, Lanahan A, Buck CR, Sehgal A, Morgan A, Mercer E, Bothwell M, Chao M (1986). Expression and structure of the human NGF receptor. 47:545-554
Kaplan DR, Hempstead BL, Martin-Zanca D, Chao MV, Parada LF (1991). The trk proto-oncogene product: a signal transducing receptor for nerve growth factor. Science 252:554–558.
Klein R, Jing SQ, Nanduri V, O'Rourke E, Barbacid M (1991). The trk proto-oncogene encodes a receptor for nerve growth factor. Cell 65:189–97.
话题:
0
推荐
财新博客版权声明:财新博客所发布文章及图片之版权属博主本人及/或相关权利人所有,未经博主及/或相关权利人单独授权,任何网站、平面媒体不得予以转载。财新网对相关媒体的网站信息内容转载授权并不包括财新博客的文章及图片。博客文章均为作者个人观点,不代表财新网的立场和观点。




 京公网安备 11010502034662号
京公网安备 11010502034662号 